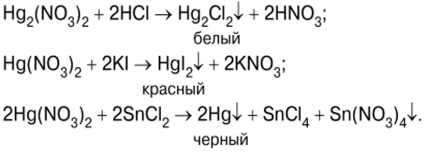
تفاعلات مركبات الزئبق
يعتبر الزئبق المعدني ومركباته شديد السمية للكائنات الحية. هذا ينطبق بشكل خاص على المركبات عالية الذوبان في الماء. يجب توخي الحذر الشديد عند تجربة تركيبات هذا العنصر الفريد (الزئبق هو المعدن الوحيد السائل في درجة حرارة الغرفة). الامتثال للمبادئ الأساسية للكيميائي؟ سيسمح لك بإجراء العديد من التجارب بأمان مع مركبات الزئبق.
في التجربة الأولى ، حصلنا على ملغم الألومنيوم (محلول من هذا المعدن في الزئبق السائل). محلول الزئبق (الثاني) نترات الزئبق (V) Hg (NO3)2 وقطعة من أسلاك الألمنيوم (الصورة 1). يتم وضع قضيب من الألومنيوم (تم تنظيفه بعناية من الرواسب) في أنبوب اختبار بمحلول ملح زئبقي قابل للذوبان (الصورة 2). بعد مرور بعض الوقت ، يمكننا ملاحظة انطلاق فقاعات الغاز من سطح السلك (الصورتان 3 و 4). بعد إزالة القضيب من المحلول ، اتضح أن الطين مغطى بطبقة رقيقة ، بالإضافة إلى ذلك ، نرى أيضًا كرات من الزئبق المعدني (الصورتان 5 و 6).
الكيمياء - تجربة الجمع بين الزئبق
في ظل الظروف العادية ، يتم طلاء سطح الألومنيوم بطبقة محكمة من أكسيد الألومنيوم.2O3يعزل المعدن بشكل فعال عن التأثيرات البيئية العدوانية. بعد تنظيف القضيب وغمره في محلول من ملح الزئبق ، يتم إزاحة أيونات الزئبق2+ ألومنيوم أكثر نشاطًا
يشكل الزئبق المترسب على سطح القضيب ملغمًا من الألمنيوم ، مما يجعل من الصعب على الأكسيد الالتصاق به. الألومنيوم معدن نشط للغاية (يتفاعل مع الماء لتحرير فقاعات الهيدروجين والغاز) ، واستخدامه كمادة هيكلية ممكن بسبب طلاء الأكسيد الكثيف.
في التجربة الثانية ، سنكتشف أيونات الأمونيوم NH.4+ باستخدام كاشف نيسلر (الكيميائي الألماني جوليوس نيسلر كان أول من استخدمه في التحليل عام 1856).
جرب تفاعل القفزات ومركبات الزئبق
يبدأ الاختبار بترسيب الزئبق (II) يوديد HgI.2، بعد خلط محاليل يوديد البوتاسيوم KI ونترات الزئبق (II) (V) Hg (NO3)2 (الصورة 7):
الراسب البرتقالي والأحمر من HgI2 (الصورة 8) ثم تعامل مع فائض من محلول يوديد البوتاسيوم للحصول على مركب مركب قابل للذوبان من الصيغة K2زئبق4 ؟ رباعي كلوريد البوتاسيوم (II) (الصورة 9) ، وهو كاشف نيسلر:
باستخدام المركب الناتج ، يمكننا اكتشاف أيونات الأمونيوم. ستظل هناك حاجة إلى حلول هيدروكسيد الصوديوم NaOH وكلوريد الأمونيوم NH.4Cl (الصورة 10). بعد إضافة كمية صغيرة من محلول ملح الأمونيوم إلى كاشف نيسلر وقلوية الوسط بقاعدة قوية ، نلاحظ تكوين محتويات أنبوب الاختبار باللون الأصفر البرتقالي. يمكن كتابة رد الفعل الحالي على النحو التالي:
مركب الزئبق الناتج له هيكل معقد:
يستخدم اختبار نيسلر شديد الحساسية لاكتشاف حتى آثار أملاح الأمونيوم أو الأمونيا في الماء (مثل ماء الصنبور).

