كيف تعمل بطارية ليثيوم أيون لسيارة كهربائية؟
بعد أن رأينا في مقال آخر عمل بطارية الرصاص التي تم تجهيز جميع السيارات بها ، فلنلقِ نظرة الآن على مبدأ تشغيل السيارة الكهربائية وخاصة بطارية الليثيوم ...

أمير
كما هو الحال مع أي نوع من البطاريات ، يظل المبدأ كما هو: أي توليد الطاقة (هنا الكهرباء) نتيجة تفاعل كيميائي أو حتى كهربائي ، لأن الكيمياء دائمًا بجانب الكهرباء. في الواقع ، الذرات نفسها مصنوعة من الكهرباء: هذه هي الإلكترونات التي تدور حول النواة والتي تشكل بطريقة ما "غلاف" الذرة ، أو حتى "قشرتها". مع العلم أيضًا أن الإلكترونات الحرة تطير بقطع من الجلد تقضي وقتها في الانتقال من ذرة إلى أخرى (دون الالتصاق بها) ، هذا فقط في حالة المواد الموصلة (يعتمد على عدد طبقات الإلكترونات وعدد الإلكترونات في آخر قذيفة).
ثم نأخذ "قطعة من الجلد" من الذرات (ومن ثم بعض الكهرباء) من خلال تفاعل كيميائي لإنتاج الكهرباء.

الأساسيات
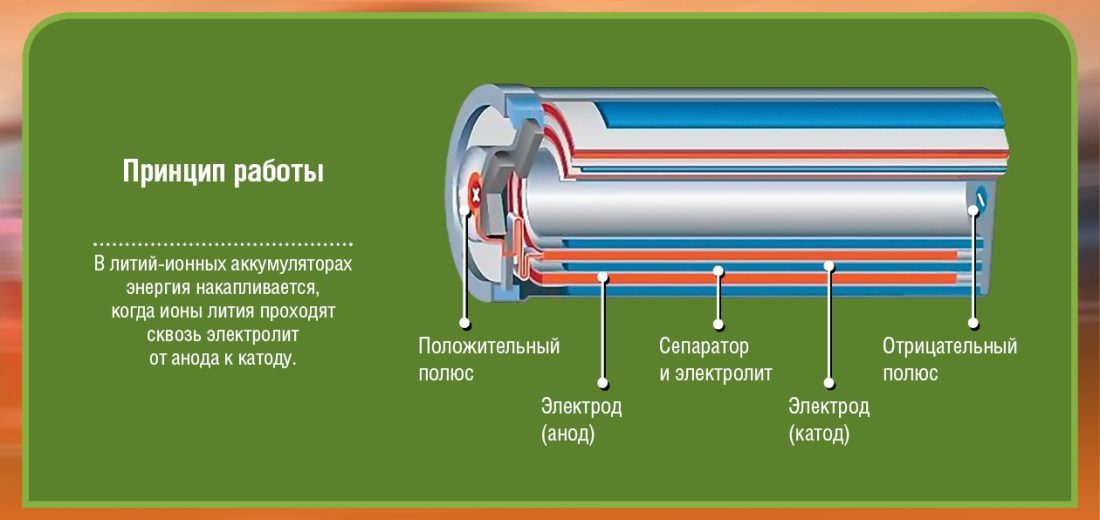
بادئ ذي بدء ، هناك قطبان (أقطاب كهربائية) نسميهما أشعة الكاثود (+ طرفي: في أكسيد الليثيوم الكوبالت) و الأنود (المحطة -: الكربون). يتكون كل من هذه الأقطاب من مادة إما تنحرف الإلكترونات (-) أو تجذب (+). غمرت المياه كل شيء بالكهرباء مما يجعل من الممكن حدوث تفاعل كيميائي (نقل مادة من القطب الموجب إلى القطب السالب) نتيجة لتوليد الكهرباء. يتم إدخال حاجز بين هذين القطبين (الأنود والكاثود) لتجنب الدوائر القصيرة.
يرجى ملاحظة أن البطارية تتكون من عدة خلايا ، كل منها يتكون من ما هو مرئي في المخططات. على سبيل المثال ، إذا جمعت خليتين من 2 فولت ، فسيكون لدي 2 فولت فقط عند إخراج البطارية. لتحريك سيارة تزن عدة مئات من الكيلوجرامات ، تخيل عدد الخلايا المطلوبة ...
ماذا يحدث في المكب؟
على اليمين توجد ذرات الليثيوم. يتم تقديمها بالتفصيل ، حيث يمثل القلب الأصفر البروتونات والقلب الأخضر يمثل الإلكترونات التي تدور حولها.
عندما تكون البطارية مشحونة بالكامل ، تكون جميع ذرات الليثيوم على جانب الأنود (-). تتكون هذه الذرات من نواة (مكونة من عدة بروتونات) ، لها قوة كهربائية موجبة مقدارها 3 ، وإلكترونات لها قوة كهربائية سالبة قدرها 3 (1 في المجموع ، لأن 3 × 3 = 1). ... لذلك ، فإن الذرة مستقرة مع 3 موجبة و 3 سلبية (لا تجذب أو تنحرف الإلكترونات).
نقوم بفصل إلكترون عن الليثيوم ، والذي يتضح أنه مع اثنين فقط: ثم ينجذب إلى + ويمر عبر القسم.
عندما أقوم بالاتصال بين طرفي + و - (لذلك عندما أستخدم بطارية) ، ستنتقل الإلكترونات من الطرف - إلى الطرف + على طول السلك الكهربائي الخارجي للبطارية. ومع ذلك ، فإن هذه الإلكترونات تأتي من "شعر" ذرات الليثيوم! بشكل أساسي ، من بين الإلكترونات الثلاثة التي تدور حولها ، يتمزق 3 ويتبقى للذرة 1. فجأة ، لم تعد قوتها الكهربائية متوازنة ، مما يؤدي أيضًا إلى تفاعل كيميائي. لاحظ أيضًا أن ذرة الليثيوم تصبح أيون الليثيوم + لأنه الآن موجب (3 - 2 = 1 / النواة تساوي 3 والإلكترونات تساوي 2 ، لأننا فقدنا واحدًا. الجمع يعطي 1 ، وليس 0 كما كان من قبل. لذلك لم يعد محايدًا).
سيؤدي التفاعل الكيميائي الناتج عن عدم التوازن (بعد كسر الإلكترونات لتوليد التيار) إلى الإرسال أيون الليثيوم + إلى الكاثود (طرفي +) من خلال الجدار المصمم لعزل كل شيء. في النهاية ، تنتهي الإلكترونات والأيونات + في الجانب +.
في نهاية التفاعل ، يتم تفريغ البطارية. يوجد الآن توازن بين طرفي + و - ، مما يمنع الكهرباء الآن. في الأساس ، يتمثل المبدأ في إحداث اكتئاب على المستوى الكيميائي / الكهربائي من أجل توليد تيار كهربائي. يمكننا أن نفكر في هذا على أنه نهر ، فكلما زاد انحداره ، زادت أهمية شدة تدفق المياه. من ناحية أخرى ، إذا كان النهر مسطحًا ، فلن يتدفق بعد الآن ، مما يعني نفاد البطارية.
تعبئة رصيد؟
تتكون إعادة الشحن من عكس العملية عن طريق حقن الإلكترونات في اتجاه - وإزالة المزيد عن طريق الشفط (يشبه إلى حد ما تجديد مياه النهر لاستخدام تدفقه مرة أخرى). وبذلك يتم استعادة كل شيء في البطارية كما كان قبل تفريغها.
في الأساس ، عندما نقوم بالتفريغ ، نستخدم تفاعلًا كيميائيًا ، وعندما نقوم بإعادة الشحن ، نعيد الأشياء الأصلية (ولكن من أجل ذلك تحتاج إلى طاقة وبالتالي إلى محطة شحن).
يرتدي؟
تتلف بطاريات الليثيوم بشكل أسرع من بطاريات الرصاص الحمضية القديمة الجيدة التي تم استخدامها في سياراتنا لعدة قرون. يميل المنحل بالكهرباء إلى التحلل ، مثل الأقطاب الكهربائية (الأنود والكاثود) ، ولكن يجب أيضًا أن يؤخذ في الاعتبار أن الرواسب تتشكل على الأقطاب الكهربائية ، مما يقلل من انتقال الأيونات من جانب إلى آخر ... تسمح لك الأجهزة الخاصة لاستعادة البطاريات المستعملة بتفريغها بطريقة خاصة.
يقدر عدد الدورات الممكنة (التفريغ + إعادة الشحن الكامل) بحوالي 1000-1500 ، بحيث يكون نصف الدورة عند إعادة الشحن من 50 إلى 100٪ بدلاً من 0 إلى 100٪. يؤدي التسخين أيضًا إلى إتلاف بطاريات الليثيوم أيون بشدة ، والتي تميل إلى أن تصبح ساخنة عند سحب الكثير من الطاقة.
انظر أيضًا: كيف أحفظ البطارية في سيارتي الكهربائية؟
قوة المحرك والبطارية ...
على عكس المصور الحراري ، لا تتأثر الطاقة بخزان الوقود. إذا كان لديك محرك بقوة 400 حصان ، فإن امتلاكك لخزان سعة 10 لترات لن يمنعك من الحصول على 400 حصان ، حتى لو كان ذلك لفترة قصيرة جدًا ... بالنسبة للسيارة الكهربائية ، فإن الأمر مختلف تمامًا! إذا لم تكن البطارية قوية بما فيه الكفاية ، فلن يكون المحرك قادرًا على العمل بكامل طاقته ... هذا هو الحال مع بعض الطرز حيث لا يمكن دفع المحرك أبدًا إلى أقصى حدوده (إلا عندما يعبث المالك ويضيف عيارًا كبيرًا البطارية!).
الآن دعنا نكتشف: كيف يعمل المحرك الكهربائي
كل التعليقات وردود الفعل
Dernier تم نشر التعليق:
ماو (التاريخ: 2021 ، 03:03:15)
عمل جيد جدا
Il أنا. 1 رد الفعل (ردود) على هذا التعليق:
- مدير مدير الموقع (2021-03-03 17:03:50): هذا التعليق أفضل 😉
(ستكون مشاركتك مرئية تحت التعليق بعد التحقق)
اكتب تعليق
ما هو شعورك حيال أرقام الاستهلاك المعلنة من قبل الشركات المصنعة؟
